
Tokom protekle decenije, naši testovi su procenjeni kroz opsežna klinička ispitivanja i saradnja u istraživanju što je rezultiralo stotinama publikacija koje pokazuju prognostičku sposobnost i kliničku korisnost MammaPrint i BluePrint.
MammaPrint je podržan od najvišeg nivoa kliničkih dokaza (nivo 1A) iz MINDACT-a,1 značajnog nezavisnog ispitivanja objavljenog u Nev England Journal of Medicine 2016. godine.
MINDACT označava (Microarray In Node-negative Disease may Avoid ChemoTherapy) Mikroniz kod limfnih čvor negativnih pacijenata koji utiče na čvor (ili 1-3 pozitivna limfna čvora) pa može izbeći hemoterapiju. To je faza III, prospektivna, eksperimentalna, klinička studija za test recidiva raka dojke.
Ispitivanjem se istraživalo klinička korisnost MammaPrint-a, u poređenju sa (ili zajedno sa) standardnim patološkim kriterijumima za izbor pacijenata za koje je malo verovatno da će imati koristi od adjuvantne hemoterapije.
Učesnici su kategorisani kao nisko ili visoko rizični od recidiva raka na dva načina: prvo, analizom tumorskog tkiva pomoću MammaPrint; i drugo, koristeći Adjuvant! Online, alat koji izračunava rizik od recidiva raka dojke na osnovu uobičajenih kliničkopatoloških faktora.
Pacijenti koji su okarakterisani kao nisko rizični sa obe kliničke i genomske procene bili su pošteđeni hemoterapije, dok je pacijentima koji su okarakterisani kao visoko rizični kod obe savetovano da se podvrgnu hemoterapiji. Oni koji imaju neusklađene rezultate randomizovani su da koriste ili kliničku ili genomsku (MammaPrint) procenu rizika da bi se odlučili na lečenje hemoterapijom.
MINDACT nalazi
klinički visoko rizičnih kod MINDACT-a, MammaPrint je klasifikovao kao genomski nisko rizične i zbog toga su mogli biti pošteđeni adjuvantne hemoterapije.
za klinički visoko rizične pacijente koje je MammaPrint reklasifikovao kao genomski nisko rizične, 95% je bilo bez udaljenih metastaza * tokom 5 godina bez hemoterapije
za pacijente koji su bili klinički visoko rizični, ali MammaPrint nisko rizični sa 1-3 uključenih limfnih čvorova, 96% je bilo bez udaljenih metastaza * tokom 5 godina bez hemoterapije
PROMIS
test
U 2015. godini, PROMIS2 (Prospektivno Istraživanje MammaPrint-a kod Pacijenata sa Karcinomom Dojke sa Prosečnom Ocenom Recidiva) ocenilo je 840 pacijenata sa karcinomom dojke u ranom stadijumu, koji su dobili „srednji“ rezultat recidiva iz onkotip DX genomskog testa. Cilj je bio proceniti promenu u odlukama lekara nakon primanja rezultata MammaPrint.
klinički visoko rizičnih kod MINDACT-a, MammaPrint je klasifikovao kao genomski nisko rizične i zbog toga su mogli biti pošteđeni adjuvantne hemoterapije.
za klinički visoko rizične pacijente koje je MammaPrint reklasifikovao kao genomski nisko rizične, 95% je bilo bez udaljenih metastaza * tokom 5 godina bez hemoterapije
za pacijente koji su bili klinički visoko rizični, ali MammaPrint nisko rizični sa 1-3 uključenih limfnih čvorova, 96% je bilo bez udaljenih metastaza * tokom 5 godina bez hemoterapije
Kada su analizirali podgrupu od 368 pacijenata kod kojih je originalna preporuka lečenja (zasnovana na onkotipnom DKS intermedijarnom rezultatu) bila u sukobu sa onom koju je naznačio MammaPrint, 76% pacijenata je promenilo plan lečenja, uz dodavanje ili uklanjanje hemoterapije.
Autori studije su zaključili da MammaPrint pruža klinički prihvatljive informacije o pacijentima koji su klasifikovani kao srednji rizik testom Oncotipe DKS (21-genski potpis) i da lekari mogu razmotriti upotrebu MammaPrint-a kako bi pomogao u odlučivanju o lečenju ovih pacijenata.
U 79% slučajeva lekari su imali veće poverenje u svoje preporuke za lečenje na osnovu rezultata MammaPrint.
STO-3 test
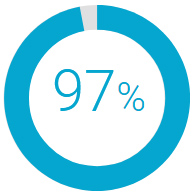
20-godišnji opstanak specifičan za karcinom dojke sa ograničenom hormonskom terapijom
U studiji3 objavljenoj 2017. godine, MammaPrint je korišćen za analizu 652 uzorka pacijenata sa 20-godišnjim podacima praćenja iz budućeg†, randomiziranog‡ Stockholm Tamokifen Testa.
Pokazalo se da bi novi MammaPrint prag mogao da identifikuje podgrupu pacijenata sa izuzetno niskim rizikom od recidiva raka 20 godina nakon dijagnoze (Kasni recidiv (20 godina), mali rizik).
Ove pacijentkinje, od kojih je većina primala samo dve godine lečenja tamoksifenom, imale su 20-godišnji opstanak specifičnog preživljavanja raka dojke od 97%. Pacijenti sa rezultatom niskog rizika kasnih recidiva (20 godina) koji nisu primili nijedan tretman posle operacije (ni hemoterapiju ni hormonsku terapiju) imali su 94% specifične stope preživljavanja kod raka dojke.
Ove informacije mogu biti od pomoći lekarima u odlučivanju da li preporučiti produženu, standardnu ili ograničenu hormonsku terapiju određenim pacijentima. Lekarima i njihovim pacijentima pruža više mogućnosti za bolje upravljanje bolešću.
Napomena: Za pristup rezultatima probnog postupka za STO potrebna je pretplata na JAMA ili OpenAthens ili Shibboleth. Za više informacija o ispitivanju kontaktirajte nas putem e-maila na customerservice@agendia.com.
*Vreme do pojave udaljenih metastaza. Metastaza na daljinu odnosi se na rak koji se sa originalnog tumora proširio na udaljene organe.
†Perspektivna se odnosi na to kada se pacijenti angažuju u kliničkoj studiji i prate ih na vreme.
‡Randomizacija je postupak za raspodelu učesnika kliničke studije u različite grupe. Koristeći šansu da rasporedite učesnike, grupe će verovatno biti slične i dozvoljavaju da se efekti tretmana uporede pravednije.
REFERENCE
1Cardoso F, van Veer LJ, Bogaerts J, et al. 70-genski potpis kao pomoć pri odlučivanju o lečenju u ranom dobu. N Engl J Med. 2016; 375 (8): 717-29
2Tsai M, Lo S, Audeh V i dr. Udruživanje nalaza ispitivanja gena od 70 gena sa lekarima za lečenje pacijenata sa ranim karcinomom dojke klasifikovanim kao srednji rizik od strane analize 21 gena. JAMA Oncol. 2018; 4 (1): e173470
3Esserman LJ, Iau C, Thompson CK i dr. Upotreba molekulskih alata za identifikaciju pacijenata sa indolentnim karcinomom dojke sa veoma malim rizikom tokom dve decenije. JAMA Oncol. 2017; 3 (11): 1503-1510
